根據公司網站,目前推動之自體樹突細胞/腫瘤抗原(ADCTA-SSI-G1)免疫療法輔助復發性惡性神經膠質腦瘤(GBM)臨床試驗計畫已於2019年4月獲得衛生衛福部食物藥品管理署(TEDA)核准,正式進入第三期臨床實驗。
本試驗「自體樹突細胞/腫瘤抗原(ADCTA-SSI-G1)免疫療法輔助復發性惡性神經膠
質腦瘤(GBM)現行標準治療之療效探討:一項多中心、開放式、隨機分配之第三期
臨床試驗」,連結林口長庚紀念醫院、基隆長庚紀念醫院、嘉義長庚紀念醫院、高
雄長庚紀念醫院、台中榮民總醫院、台南奇美醫院及成功大學附設醫院共七個醫學
中心及十二位專業資深臨床醫師,預計收案118病患,希望延續先前第一/二期與第
二期臨床試驗之臨床應用經驗,成為GBM免疫輔助治療之首選治療方案。
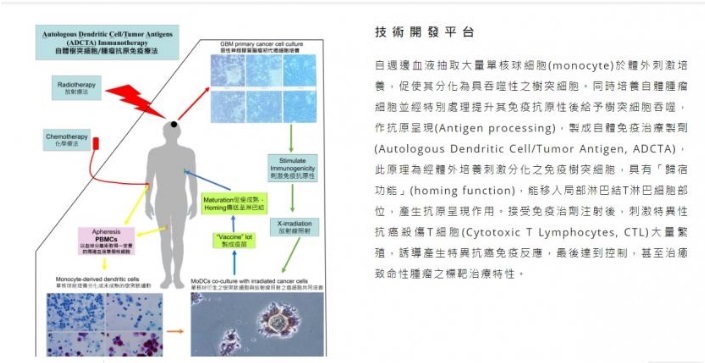
資料來源:http://www.genetinfo.com/investment/featured/item/34922.html